摘要
在仿制药研发过程中,除对仿制药进行技术、临床、市场和注册策略进行评估外,专利信息问题也是仿制药立项过程需要重点关注的话题,例如,目标仿制药都涉及哪些专利,专利在目标市场国的保护情况,目标仿制药是否构成侵权等。本文主要介绍了专利信息在仿制药研发中的应用,以期为国内仿制药企业提供参考。
正文
专利是除期刊文献之外非常重要的技术信息来源渠道,通过对专利信息的分析与研究,不仅可以使企业降低侵权风险,避免重复研究,节约研究时间和经费,还可以通过专利信息中的技术方案信息为仿制药企业技术人员开拓视野,提高创新点,并了解原研企业的研发动向。
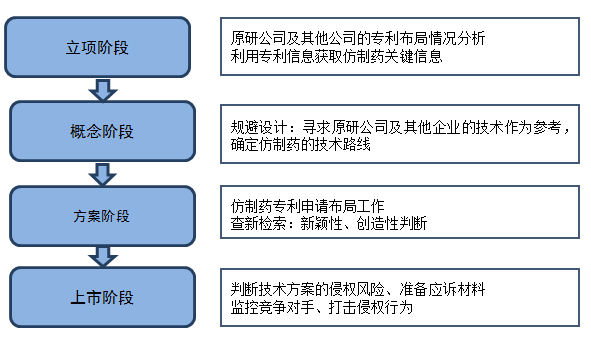
从研发项目管理的角度看,可以将仿制药的研发分为如下几个阶段,即立项阶段、概念阶段、方案阶段、上市及产业化阶段。每个阶段都有相应的评审和交付物,例如,立项阶段会有立项报告,其中会涉及药物基本信息、市场信息、知识产权信息等内容,概念阶段会有概念设计方案,方案阶段会有整体方案和详细方案,上市及产业化阶段有上市分析报告。大部分仿制药企业在产品开发过程中一般注重成本、技术、质量等方面,而忽视对专利信息的关注。
如何在仿制药研发过程中有效利用专利信息是很多企业面临的问题。事实上,在仿制药研发的各个阶段都离不开对于专利信息的利用分析,具体而言,从项目立项时就应该进行专利分析,然后到产品的整体方案设计、详细方案设计和最终产品的上市阶段都要进行专利信息的分析。
一、立项阶段
在仿制药立项阶段,仿制药企业需要仔细调研和分析原研公司及其他制药公司的专利情况及专利布局情况。一般来讲,药品所涉及的专利类型有化合物通式专利、化合物专利、晶型专利、适应症专利、组合物专利、联合用药专利、制备方法专利、中间体专利等。药品就是通过上述不同类型的专利从多维度得以保护,立项过程中需要对以上不同类型的专利进行逐一梳理,从而为仿制药立项决策提供依据。
另一方面,在仿制药立项阶段,仿制药企业可通过专利信息来间接获取相应的仿制药信息(例如晶型信息、制剂处方信息、制备工艺信息等)。
下文以立普妥的处方为例做简要说明。仿制药企业在仿制药的研发初期需要调研仿制药的基本信息,通常仿制药企业可以通过Drugs@FDA、橙皮书、Drugfuture等数据库初步确定原研药的处方。为了了解立普妥的处方信息,仿制药企业可通过FDA官网的Drug@FDA数据库查询立普妥的说明书(labels)。通过阅读说明书找出立普妥片剂的辅料成分为:碳酸钙、小烛树蜡、交联羧甲基纤维素钠、羟丙基纤维素、单水合乳糖、硬脂酸镁、微晶纤维素、欧巴代白YS1-7040(羟丙基甲基纤维素、聚乙二醇、滑石粉、二氧化钛)、吐温80和二甲基硅油乳液。

然而Drug@FDA数据库收录的处方信息仅包含药物和辅料的种类,不含这些成分的具体含量,因此还需借助原研药专利中记载的信息进一步了解处方各成分的含量。
经查询专利US6126971A的实施例1中公开了立普妥片剂的制备工艺以及各种成分的使用量。


需要说明的是,这些专利中公开的信息可能与原研药实际生产中使用的处方组成、物质含量和工艺存在差异,因此这些实施例仅可作为参考使用。例如,上述实施例公开的处方中并未涉及药品说明书中提及的小烛树蜡、欧巴代白YS1-7040和二甲基硅油乳液。因此,仿制药企业在确定药品处方时应综合考虑专利说明书与原研药说明书公开的信息进行匹配和验证。
二、概念阶段
概念阶段主要是拟定仿制药品种的开发思路和工艺路线。目前我国大多仍采用“仿创结合”的药品开发模式。当仿制药品种的基本药物专利保护期到期后,其后续的制备方法、晶型和制剂等外围专利尚在保护期内,若想要提前进入仿制药市场,则需要仿制药企业进行规避设计和再次创新来突破相关外围专利的技术壁垒。
通常针对原研药的创新研发策略主要有:(1)模拟创新,通过对药物晶型进行研发,开发出新的晶型,从而避开原研专利保护的范围;(2)改进创新,通过改进原研药物的合成工艺、制剂和质量控制方法,为日后的注册报批做好准备。一般来讲,仿制药企业一般在原研药物的化合物专利文献公开后即启动模拟创新的研发工作[1],而对于合成工艺和制剂的改进则一般是在化合物专利临近到期前才开始启动。
在进行规避设计时,仿制药企业可以针对特定的技术进行专利检索,从公开的专利信息中了解原研公司和其他公司的技术设计方案,并进行技术参考,从而进行替换性方案开发或者进一步的改进开发。由于专利信息包括对于一个详细技术方案的公开,因而在技术参考时能够提供更为具体的启迪作用。
三、方案阶段
方案阶段是指仿制药在仿制药研发过程中产生具体详细方案本身的阶段,这个阶段的专利信息工作重点主要体现为两个方面,一是充分利用专利文献,找出仿制药研发过程中的发明点,并进行新颖性、创造性判断,二是进行专利申请布局工作。
在专利文献利用方面,可通过阅读专利文献启发设计思路,促进发明点的设计,同时对仿制药研发过程中产出的技术方案进行查新检索(新颖性、创造性判断),通过查新检索一方面可以判断拟专利申请的授权前景,另一方面可以指导专利的进一步挖掘。
在专利申请布局方面,大多数仿制药企业采取的专利布局策略是对原研化合物的外围专利进行规避设计及专利布局,通常晶型专利、药物制剂专利、制备方法专利等外围专利是仿制药企业的布局重点。
在仿制药开发过程中,药物晶型专利是仿制药企业首先考虑的问题,也是仿制药企业进行规避设计和专利布局的重点。晶型己经成为创新和仿制化学药物研究的重要技术环节,晶型质量也越来越受到国际药学界的广泛重视。究其原因,一方面新晶型专利是提升药品质量与保持药品市场竞争能力的核心关键技术,也是破解原研药企利用外围专利延长专利期限的利器;另一方面,国际上各原研公司一般在化合物专利推出5-6年后[2]才推出晶型专利,这也为仿制药企业在药物新晶型的争夺战中预留了空间,谁能在专利药的制备工艺之外仿制出一种新的晶型无疑在争夺仿制药资格方面占据领先地位。
除晶型专利之外,药物制剂也是仿制药企业进行专利布局的重点,仿制药企业可通过减少剂量、易用性、改善治疗效果、降低副作用等特征来开发和申请新的制剂专利,包括现有药物的缓释制剂、长效制剂、崩解剂型等[3]。
一种化合物可经多种合成方法获得,因此,制备方法研究是仿制药企业研发的另一重点,立项时也可对于专利文献中的合成方法进行仔细评估,在已公开的合成路线基础上进行优化设计,最后从杂质、收率、成本等多因素加以综合考虑并确定颇占优势的合成路线作为所采用和拟保护的工艺开发路线。
四、上市阶段
上市阶段分为上市前和上市后两个子阶段。
上市前,仿制药企业需要对仿制药产品所涉及的相关专利进行补充检索并判断侵权风险(FTO),以确保上市后面临的侵权风险在可控范围内。
仿制药企业进行FTO检索分析时,需要注意以下几个方面:
①专利的法律层面,专利的保护范围以授权专利文本的有效权利要求书为准。
②我国目前对药品专利的保护期尚未延长,授权专利的保护期限自申请日起20年。所有涉及“发明专利申请公布后的视为撤回”,“发明专利申请公布后的驳回”,“专利权终止”等的申请或专利均处于失效状态,这些申请或专利对于仿制药的开发不会造成实质性影响。
③专利的法律状态是一个动态变化过程,需要随时针对与被仿制药的相关专利在中国的法律状态进行更新。还应随时跟进原研公司或仿制药公司后续申请的相关专利情况。
上市后,仿制药产品的市场占有率有所增加并获得了一定的知名度,这时专利信息的利用工作主要有两个方面,一方面是监控竞争对手,发现侵权对象,用以提起侵权诉讼打击同质化竞争行为[4],第二方面是准备应诉材料,即对存在侵权风险的专利提前准备无效证据/理由。此外,还应实时跟踪原研公司及其他药企新公开的专利申请和新授权的专利,对有潜在威胁的专利申请提出公众意见和对已经授权的专利进行无效准备工作等。
五、结语
通过上述分析可以看出,专利信息检索、分析和侵权判断是一项十分复杂并耗时耗力的工程。在整个仿制药开发过程中,仿制药企业应将专利检索分析融入到仿制药研发管理的整个历程中,同时建立专利跟踪检索预警分析机制,重点关注跟踪所仿制药品的专利申请、审查、无效、侵权的相关动态,以规避重复研发、规避侵权风险、同时挖掘和布局自有的衍生专利,为研发提供技术支撑,推动项目进展。
[1] 杨倩,马秋娟,汪小涧.从专利视角谈药物二次创新与仿制药开发——以HIV蛋白酶抑制剂洛匹那韦为例 [J].中国药科大学学报,2015,46(04):499-503.
[2] 石瑛.从头孢地尼专利案透析国外仿制药公司研发争霸战[J].世界临床药物,2008,29(09):568-570.
[3]纪媛媛,周东明.从知识产权角度浅析仿制药企业的发展之道[J].中国新药杂志,2016,25(11):1212-1215.
[4]张辉,刘桂英.仿制药企业的专利策略探析[J].中国新药杂志,2014,23(01):11-16.